کلسیم کلرید (CaCl2) چیست؟ این ترکیب شیمیایی که با نام کلسیم دی کلرید نیز شناخته می شود، کاربردهای گسترده ای در صنعت و مصارف خانگی دارد. کلسیم کلرید یا نمک کلسیم نوعی هالید یونی است که در دسته مواد معدنی قرار می گیرد. در دمای اتاق جامد است. می تواند به صورت هیدراته نیز باشد که تعداد مولکول های آب آن از صفر تا شش عدد متغیر است. این نمک یک ترکیب اعجاب انگیز است که از مهم ترین ویژگی های آن می توان به کنترل گرد و غبار، رطوبت گیری قوی و ضد یخ بودن عالی اشاره کرد.صنایع شیمیایی تهران در زمینه فروش کلسیم کلرید در گریدهای صنعتی، آزمایشگاهی و خوراکی آماده پاسخ به مشتریان عزیز می باشد.
خرید کلسیم کلرید
جهت استعلام قیمت کلسیم کلرید با کارشناسان ما تماس بگیرید و یا از طریق فرم بالا سفارش خود را ثبت نمایید.
خواص فیزیکی و شیمیایی
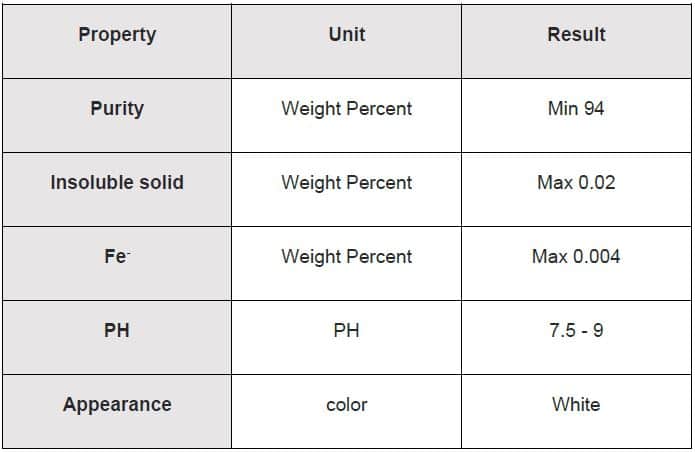
این ترکیب معمولا به صورت کریستال های سفید رنگ و بدون بو با ساختار هشت وجهی (کیوبیک) است. کلسیم کلرید جاذب رطوبت است و به دو صورت خشک و هیدراته وجود دارد اما نوع دی هیدرات و هگزا هیدرات آن بسیار نادر است. برخلاف سایر ترکیبات کلسیم، این نمک بسیار محلول است و می توان از آن به منبع یون کلسیم استفاده کرد. در گلیسیرین محلول است و وقتی آن را با غلظت بالا در گلیسیرین حل می کنند به صورت شیشه ای در می آیند.
| فرمول شیمیایی | CaCl2 |
| وزن مولکولی | 110.978 گرم بر مول |
| نقطه جوش | 1670 درجه سانتی گراد |
| نقطه ذوب | 782 درجه سانتی گراد |
| حلالیت | در آب در حدود 0.745 گرم بر میلی لیتر در دمای 20 درجه سانتی گراد |
| چگالی | 2.15 در دمای 68 درجه فارنهایت |
| نقطه جوش |
1600 درجه سانتی گراد |
روش تولید کلرید کلسیم
- فرآیند Solvay: در این فرآیند از واکنش کربنات کلسیم و سدیم کلرید استفاده می شود تا محصول بی کربنات سدیم و CaCl2 تولید شود. با استفاده از این روش می توان این ترکیب را با غلظت های مختلف و به شکل خشک و یا هیدراته را تهیه کرد.
CaCo3 + 2NaCl → Na2CO3 + CaCl2
- فرآیند HCl: این نمک به صورت طبیعی در فرم های هیدراته خود در طبیعت به وجود می آید. کلسیم کلرید به طور عمده با واکنش سنگ آهک با فرمول مولکولی CaCO3 و اسید کلریدریک با فرمول مولکولی HCl به وجود می آید.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
- دریاچه های نمک طبیعی: غالباً از منابع زیرزمینی که به طور طبیعی وجود دارند می توان کلسیم کلرید را استخراج می شود. برای این کار از تصفیه دریاچه های نمکی استفاده می کنند که در آن کلسیم هیدروکسید را به محلول اضافه می کنند در نتیجه آن رسوب کلسیم کلرید ایجاد می شود. می توان غلظت آن را با تبخیر آب افزایش داد.
واکنش های کلرید کلسیم
واکنش با سدیم فسفات
این نمک می تواند با سدیم فسفات ترکیب شود و با آن واکنش دهد. واکنش آن از نوع جابجایی دوگانه بوده و محصول آن کلسیم فسفات و سدیم کلرید می باشد.
3CaCl2+2NaPo4→Ca3(Po4)2+6NaCl
واکنش کلسیم کلرید با آب
کلسیم کلرید یک ترکیب نمکی است که براحتی در آب حل می شود. در نتیجه تجزیه آن کلسیم هیدروکسید و اسید کلریدریک تولید می شود. معادله واکنش کلسیم کلرید در آب به صورت زیر است:
CaCl2(s) → Ca2+(aq) + Cl-(aq)
CaCl2+2H2O→Ca(OH)2+2HCl
برقکافت کلسیم کلرید
برقکافت یا الکترولیز فرآیندی است که در آن مواد در اثر جریان الکتریسیته تجزیه می شوند. برقکافت کلرور کلسیم خالص و مذاب منجر به تولید عناصر سازنده آن یعنی کلسیم و کلر می شود. از انچاییکه کلسیم دارای بار مثبت است در کاتد قرار می گیرد و کلر نیز که دارای بار منفی است در آند قرار می گیرد.
هنگامی که یون های کلسیم با الکترود منفی برخورد می کنند، باتری پتانسیل کافی دارد تا بتواند این یون ها را مجبور به گرفتن الکترون برای تشکیل فلز سدیم کند.
کاتد: Ca2+ + 2e → Ca
یونهای کلر که با الکترود مثبت برخورد می کنند به گاز Cl2 اکسید می شوند و در این الکترود حباب می زنند.
آند: 2Cl- → Cl2 + 2e
اگر برقکافت در محلول آبی باشد، این بار علاوه بر کلسیم و کلر، یون های دیگری هم وجود دارد که اکساهش و کاهش انجام شود. در این حالت کلسیم به سمت کاتد و کلر به سمت آند حرکت می کند. دو ماده وجود دارد که می تواند در کاتد اکسید شود که معادلات آن به صورت زیر است:
کاتد: Ca2+ + 2e → Ca
-2H2O + 2e- → H2 + 2OH
از آنجاییکه کاهش آب نسبت به کلسیم آسان تر اتفاق می افتد، تنها محصولی که در کاتد تشکیل می شود، گاز هیدروژن است.
2H2O(l) + 2e- → H2 (g) + 2OH-(aq)
در آند نیز دو ماده وجود دارد که می تواند اکسید شوند: یون کلر و مولکول های آب.
-2Cl- → Cl2 + 2e
-2H2O → O2 + 4H+ + 4e
پتانسیل های حالت استاندارد برای این نیمه واکنش ها آنقدر به یکدیگر نزدیک است که ممکن است انتظار داشته باشیم که مخلوطی از گاز Cl2 و O2 در آند جمع آوری شود. در عمل اما، تنها محصول این واکنش Cl2 است.
-2Cl- → Cl2 + 2e
کاربرد کلرید کلسیم
این ماده شیمیایی دارای مصارف مختلفی است و بسیار شبیه به سدیم کلرید عمل می کند. به عنوان افزودنی و نگهدارنده غذا در صنعت غذایی، برای مصارف ضد یخ در جاده ها در زمستان مورد استفاده قرار می گیرد. همچنین به عنوان مواد شیمیایی استخر ها، در تصفیه آب و مصارف شیرین کردن آب نیز مورد استفاده قرار می گیرد. این ماده شیمیایی بعد از واکنش با سدیم فسفات خاصیت انحلال در آب خود را از دست خواهد داد.
کلسیم کلرید در صنعت
از این ترکیب استفاده های گسترده ای در صنعت می شود. از جمله مهم ترین کاربردهای آن در صنعت می توان به موارد زیر اشاره کرد:
- ضد یخ شیمیایی قوی برای ذوب یخ در جاده ها
- تولیدات صنعتی مانند تولید پلاستیک، مواد شیمیایی مانند پتاسیم کلرید، در تصفیه فاضلاب ها و…
- کمک به تسریع در گرفتگی و سخت شدن بتن
- استفاده در صنایع حفاری نفت و گاز
- کنترل گرد و غبار و ریزگرد ها در بیابان ها و جاده ها
عامل خشک کننده قوی
به دلیل تمایل شدید آن به جذب رطوبت هوا، این ترکیب شیمیایی در صورت قرار گرفتن در معرض اکسیژن، محلول مایع را تشکیل می دهد. این توانایی می تواند برای خشک کردن سایر مایعات آلی استفاده شود. از این رو، گاهی اوقات عامل خشك کردن نیز نامیده می شود. به دلیل جذب قوی،یک لایه از این ماده در جاده ها و در معادن به منظور کاهش مشکلات گرد و غبار استفاده می شود (کلسیم کلرید صنعتی).
ضد یخ شیمیایی قوی
این ماده در پایین آوردن نقطه ذوب و نقطه انجماد آب را کمک می کند. جاده پوشیده از یخ در مناطق سرسیر یکی از مشکلات عمده این مناطق است. جهت استفاده از این جاده ها ذوب این یخ ها بسیار مهم است. توانایی این ترکیب شیمیایی در پایین آوردن نقطه انجماد آب است که از تجمع یخ جلوگیری می کند.
عامل موثر گرمازا
این ماده شیمیایی بسیار گرمازا است. هنگامی که به مایعات اضافه می گردد، مقدار زیادی گرما آزاد می شود، دما تا 60 درجه سانتیگراد افزایش می یابد. این خصوصیت اغلب در شروع فرآیند های گرمایی در اهداف صنعتی مورد استفاده قرار می گیرد. خصوصیات جذب رطوبت هوا، انحلال فوری و خواص گرمازایی این ماده را به یکی از مواد محبوب و معروف در صنایع شیمیایی بدل کرده است.
مواد غذایی
کلسیم کلرید خوراکی به عنوان یک نگهدارنده از فاسد شدن غذا جلوگیری می کند. همچنین کمک می کند تا غذای سالم و تازه را برای مدت طولانی نگه دارید. استفاده از آن به عنوان افزودنی و نگهدارنده مواد غذایی به افزایش ارزش غذایی کمک می کند. برای حفظ استحکام و حفظ مواد غذایی کنسرو شده و جلوگیری از نرم و فاسد شدن آنها استفاده از این ماده ضروری است. گرید خوراکی این ترکیب در پنیر برای جبران کمبود کلسیم و ایجاد مزه شور مورد استفاده قرار می گیرد.
استفاده از این محصول به عنوان افزودنی غذایی مورد تایید سازمان غذا و دارو (FDA) می باشد. برخلاف کلرید پتاسیم، این ماده نمی تواند جایگزین نمک خوراکی استفاده شود، چون با مصرف طولانی باعث بیماری گوارشی می شود.
کلسیم کلرید در کشاورزی
از جمله مواد ضروری برای رشد گیاهان، کلسیم است. این ترکیب به رشد سلولی گیاهان کمک می کند و به همین دلیل در بسیاری از کودهای شیمیایی وجود دارد. از کلرور کلسیم در کودهای کشاورزی و همچنین در خوراک دام و طیور استفاده می شود. این ترکیب از ایجاد لخته در خون خیوانات و طیور جلوگیری می کند. در دوران بارداری و شیردهی دام ها نیز از این ماده در رژیم غذایی آن ها استفاده می شود.
داروسازی
تزریق این ماده در صورت بروز مواردی همچون احیای قلب, کاهش شدید کلسیم و مسمومیت با منیزیم مورد استفاده است. همچنین در درمان بیماری تتانیای هیپوکلسمیک که ناشی از افزایش غیر طبیعی کلسیم در بدن است، کاربرد دارد.
بازار خرید و فروش کلسیم کلرید
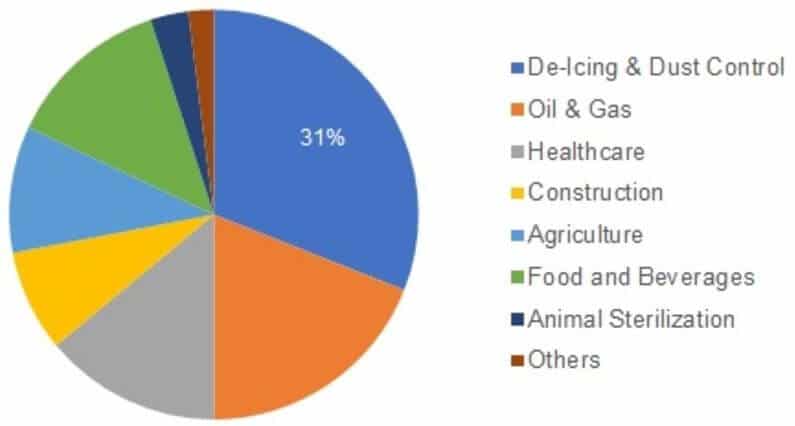
بازار جهانی این ترکیب از مرز 4 میلیون تن در سال 2017 گذشت. با رشدی حدود 4.4 درصد از سال 2010 تا 2017 رو به رو شد. یکی از دلایل مهم رشد این بازار را می توان افزایش تقاضا در حوزه محصولات ضد یخ و کنترل گرد و غبار عنوان کرد. با نگاهی به آینده این بازار می توان انتظار داشت که حجم مبادلاتی این کالا نزدیک به 5 میلیون تن در سال 2023 برسد. همچنین رشدی 3.4 درصدی را در طول سال های 2018 تا 2023 تجربه کند.
عوارض کلرید کلسیم
کلرید کلسیم خطرات جدی برای سلامتی و ایمنی به همراه دارد. بلع منجر به سوختگی در دهان و گلو، تشنگی زیاد، استفراغ، درد معده، فشار خون پایین می شود. همچنین می تواند باعث ایجاد خشکی بیش از حد یا خشک کردن پوست مرطوب شود. در موارد مواجهه شدید باعث سوختگی پوست، اختلالات قلبی، مشکلات تنفسی و تشنج می شود. به دلیل خطرات زیاد هنگام دست زدن به این مواد از روپوش، دستکش و عینک ایمنی استفاده کنید.









تیم صنایع شیمیایی تهران –
برای دریافت اطلاعات بیشتر با ما همراه باشید.